原文以The shock tactics set to shake up immunology为标题
发布在2017年5月3日的《自然》新闻专题上
原文作者:Douglas Fox
每天六次,无论在做什么,Katrin都要停下手头的事情,从衣兜里掏出一块小磁铁,用它碰碰她锁骨下面一片突起的皮肤。在一分钟内,她会感到喉咙轻微震颤,如果说话,她的声音还会有些发抖。过了一会儿,这种感觉就消退了。
这块磁铁会启动一个植入设备,释放一组脉冲电流——大概一毫安,和一般助听器使用的电流差不多,来刺激她的迷走神经。迷走神经是一束从脑干沿脖颈向下,连接着包括心脏和消化道在内的重要器官的神经。

这一植入设备可给迷走神经带来电击式刺激。该设备尚未在人体中做过测试。Patrick T. Fallon for Nature
从1990年代起,这项名叫“迷走神经刺激疗法”的技术就已被用于治疗癫痫,本世纪初又开始应用于治疗抑郁症。Katrin(化名)今年70岁,是一位居住在荷兰阿姆斯特丹市的健身教练,她使用这种疗法的目的却是控制类风湿性关节炎的病情。类风湿性关节炎是一种自体免疫性疾病,会导致关节周围的软骨和其他组织的病变。Katrin五年前参与的临床试验是该疗法的第一次人体试验,是二十多年来有关神经与免疫系统关联的研究成果的结晶。
Kevin Tracey是美国费恩斯坦医学研究所(Feinstein Institute for Medical Research)的一位神经外科医师,他认为迷走神经是神经系统和免疫系统连接中的重要一环,并表示电刺激法可能是一种较好的自体免疫疾病(红斑狼疮、克罗恩病等)疗法。
数家制药公司都在投资“电疗”(能够调节神经的设备)的研发,以治疗心血管和代谢性疾病。但Tracey的目标是用这类设备来控制炎症。倘若实现,这将是一个跨越式的重大突破。
Dianne Lorton称他为“带动许多人加入这一领域”的先锋人物,Lorton是美国肯特州立大学的神经科学家,过去三十年来,她一直在研究穿透淋巴结和脾脏等免疫器官的神经。但她和其他一些观望者提醒,人们还没有充分理解电疗抗炎作用背后的神经回路。
Tracey接受这个批评意见,但仍然认为电刺激疗法大有前景。“我们在有生之年就会见到这类设备取代一些药物”,他说。他坚持认为电击迷走神经或其他外周神经能够治疗诸多疾病,从糖尿病到高血压乃至出血。“这是一个新领域的开端。”
刺激的价值
Tracey最初走上神经免疫学道路纯属偶然。1998年,他正在研究一种编号为CNI-1493的试验性药物,它能通过降低一种名叫TNF-α(tumour-necrosis factor-α,肿瘤坏死因子α)的强效免疫蛋白的浓度来抑制动物的炎症。研究者通常会将CNI-1493注入血液系统,但有一天,Tracey突然决定将它注射进实验大鼠的脑中。他本想观察这种药物是否能在中风时降低脑中的TNF-α浓度,但实验结果却出乎他的意料。
脑中的CNI-1493降低了动物全身的TNF-α产量。其它实验表明,这一作用比直接向血液注射强大约10万倍。于是,Tracey推测这种药物在神经信号上起了作用。
他的后续实验支持了这一想法。向大鼠脑中注射CNI-1493几分钟后,Tracey便观察到一大波神经活动沿着实验大鼠的迷走神经向下传导。这条神经系统“高速公路”调控着一些无意识的生理功能,包括心率、呼吸和将食物推过消化道的肌肉收缩。Tracey推断,它或许也能控制炎症。当他切断这条神经后,药物的显著效果也随之消失了,这使他更加确信自己的推断。“这是一个颠覆性的发现”,Tracey说。它意味着如果能够直接刺激迷走神经,药物就不是必须的了。
于是,Tracey进行了一个关键实验:他向大鼠注射了致死剂量的内毒素,一种在动物中造成炎症和器官衰竭,最终导致死亡的细菌细胞壁成分。这种毒素的效果大致与人类的败血性休克一致。然后,Tracey用电极刺激了实验动物的迷走神经。接受电刺激的大鼠血液中的TNF-α含量只有未受电刺激大鼠的四分之一,而且没有发生休克。
Tracey立刻意识到了刺激迷走神经的医用价值:它能阻断TNF-α和其它引发炎症的分子含量骤升。当时,已有一些公司在销售用于治疗癫痫的植入性电刺激器,但要将这项技术拓展到治疗发炎反应,Tracey首先需要搞清楚它的作用原理和可能的副作用。
在接下来的15年里,Tracey的团队进行了一系列动物实验来探究迷走神经刺激的作用位置和机理。他们尝试了在不同位置切断神经、用药物阻滞特定神经递质等方法。这些实验似乎表明,当迷走神经受到电击时,一个神经信号会向下传导到腹部,然后经由另一条神经进入脾脏。
脾脏在免疫系统中的作用就像高速公路服务区,免疫细胞定期在这里停留休整,然后返回血液循环。Tracey团队发现,进入脾脏的神经会释放一种名叫去甲肾上腺素的神经递质,可以直接向脾脏中的T细胞(一种白细胞)传递信息。
实际上,神经细胞和T细胞的连接与神经细胞间的突触十分相像;Tracey表示,T细胞的行为方式几乎就和神经元一样。受到刺激时,T细胞会释放另一种神经递质乙酰胆碱,后者会与脾脏中的巨噬细胞结合。当动物接触到内毒素时,向血液循环大量释放TNF-α的通常就是这些免疫细胞,但暴露于乙酰胆碱则会抑制巨噬细胞释放这种炎症蛋白(见图)。
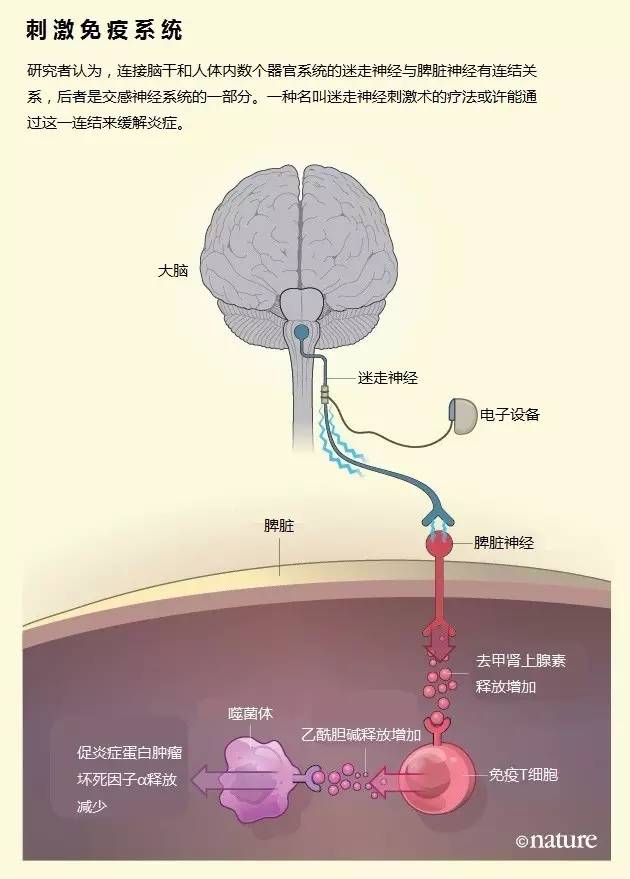
Tracey的研究成果为此前数十年的研究带来了新意义。上世纪八、九十年代,纽约罗彻斯特大学的神经解剖学家David Felten在数种动物中拍摄到了神经元-T细胞混合突触的显微图像,它们不仅如Tracey所发现的那样存在于脾脏中,在淋巴结、胸腺和肠道中也有分布。这些神经元都属于交感神经系统,负责调节机体对某些应激源的反应。Felten观察到,和Tracey在脾脏中发现的一样,这些交感神经元会通过释放去甲肾上腺素来刺激与之相配的T细胞,而且这个刺激往往都是用于减弱发炎的。
2014年,日本大阪大学的神经免疫学家中井晶子(Akiko Nakai)证实,交感神经对T细胞的刺激会限制它们从淋巴结进入循环系统,否则,它们就会在身体其它部位造成炎症。但在许多自体免疫疾病中,这种神经信号通路被打断了。
Lorton同为神经科学家的双胞胎姐妹Denise Bellinger就职于美国罗马林达大学,她们发现,在自体免疫疾病的大鼠模型中,交感神经通路有所变化,人类中也有类似的现象。过量释放的去甲肾上腺素会损害交感神经,使它们从本应调控的免疫细胞中撤出。随着疾病进展,这些神经会重新进入它们撤出的组织,然而是以异常的方式、且与不同的免疫细胞建立连结。这种重新建立的连结会持续促进炎症,而不是减缓炎症。Bellinger说,这种变化发生在脾脏、淋巴结和关节等位置,是许多疾病的病因。
但是她、Lorton以及其他研究者都对Tracey关于刺激迷走神经缓和炎症的说法表示怀疑。澳大利亚墨尔本大学的神经科学家Robin McAllen也在寻找迷走神经和脾脏中刺激T细胞的神经之间的连结,但迄今为止仍然一无所获。
刺激迷走神经是通过其它神经“起到间接作用”的,Bellinger说。她还说,先将这些神经回路的结构描绘清晰,然后再进一步将其应用于治疗人类患者非常重要:“解剖结构对可能产生的副作用有巨大影响。”
不过,即使是这些怀疑者也看到了Tracey方法的潜力。Bellinger指出,在很多自体免疫疾病中,不仅交感神经会在将自身重排入促炎症回路时变得过于活跃,对它们有拮抗作用的迷走神经也会变得活性不足。迷走神经刺激或许部分恢复了这两个神经系统间的平衡。“这是第一步,”她说,“我相信他们会将这种疗法推广到临床治疗中,而且会取得显著的成效。”
耐心试验
接受迷走神经刺激治疗癫痫或抑郁的患者可能会面临一些副作用——比如喉头疼痛、僵硬和声音发紧。在刺激自己的迷走神经时,Katrin也感到了轻微的症状。电击迷走神经也可能会造成心率减缓、胃酸分泌增加等作用。
在这方面,Tracey有理由保持乐观。人类的迷走神经包含大约10万根神经纤维,分叉连接着不同的器官。在不同神经纤维间,能引发神经活动的电量差异可高达50倍。
Tracey的前学生Yaakov Levine已经发现,参与减缓炎症反应的神经纤维激活阈值较低。它们可以被低达250微安的电流激活,这相当于一般用来抑制癫痫发作的电流强度的八分之一。另外,癫痫患者需要每天最多可达数小时的电刺激,但动物实验表明,一个简短的电刺激就能在较长时间内控制炎症。Levine介绍,受到乙酰胆碱作用后,巨噬细胞最长在24小时内不会产生再TNF-α;他如今在SetPoint Medical公司工作,这家公司的创立初衷就是将迷走神经刺激作为医疗手段商业化。
由于先前的动物研究和Levine的优化设计,到2011年,SetPoint就已准备好在人类身上试验这一技术。第一轮试验由Paul-Peter Tak监督进行,他是阿姆斯特丹大学和英国医药公司GlaxoSmithKline的风湿病学家。在几年的时间里,18位类风湿性关节炎患者被植入了刺激器,其中就包括Katrin。
在六周中,她和另外11位受试者发现症状有所减轻。进一步化验表明,他们血液中的炎症因子(比如 TNF-α和白细胞介素-6)都降低了。这些改善在关停刺激器14天后消失,然后又在重启刺激器后恢复。
自此之后,Katrin一直在使用刺激器,但每周也会注射抗风湿药物甲氨喋呤,每天服用抗炎药双氯芬酸——但她不再需要使用大剂量的免疫抑制剂类固醇了,而且她的关节好转了很多,使她得以重返工作岗位。这项试验的结果于去年七月发表在PNAS上。
另一项迷走神经刺激试验的结果也在几乎同时发表出来。法国格勒诺布尔大学医院的肠胃病学家Bruno Bonaz为七位克罗恩病患者植入了刺激器,在六个月的试验期中,五位受试者汇报症状减少,内窥镜检查也发现他们的肠道组织损伤减少了。SetPoint公司也正在进行一项临床试验,使用迷走神经刺激器来治疗克罗恩病。
Tracey和Bonaz并不是唯二希望通过驾驭神经回路来治疗炎症的研究者。加州大学圣迭戈分校的创伤外科医生Raul Coimbra研究的是败血性休克的治疗方法,这种病症每年会伤害数十万人。很多死于败血性休克的患者都被同一个原因送上了无可挽回的境地:肠道粘膜快速降解,向身体释放细菌,从而造成炎症,损伤肺、肾脏等器官。
和Tracey一样, Coimbra也通过刺激迷走神经(电击和使用一种名叫CPSI-121的试验药物都有效果),成功在动物中逆转了这种致命的过程。Coimbra希望能将这项研究推进到临床试验阶段。但他的研究也揭示了迷走神经刺激术面临的一个重要挑战:和大鼠不同,一些人类可能对这项技术有抗性。
人类基因组会编码一种多余的无功能乙酰胆碱受体蛋白,这在其它动物中是不存在的。Coimbra在加州大学圣迭戈分校的合作者Todd Costantini发现,如果这种异常受体被大量合成,神经信号传递就会受到阻碍,巨噬细胞对乙酰胆碱的响应也就随之消失。在这种情况下,即使刺激迷走神经,巨噬细胞也可能还是会继续释放TNF-α。Costantini表示,在人群中,这种蛋白的合成量有200倍的差异。他计划在人群中测试高合成量是否确实会阻碍迷走神经刺激术的抗炎效应。一些个例显示,事实很可能正如他所料。
迄今为止的小规模临床试验表明,一些人对迷走神经刺激没有反应。这种测试或许能在给患者植入刺激器前确定谁能取得较好的疗效。
不过,尽管存在这些不确定因素,“电疗”领域仍在加速发展。去年十月,美国NIH公布了刺激外周神经缓解病症(Stimulating Peripheral Activity to Relieve Conditions ,SPARC)项目。这一项目将会在2021年之前提供2.38亿美元的资金,专门支持描绘胸腔和腹腔神经回路结构的研究。
GlaxoSmithKline公司也对这一领域表示了兴趣。它已经投资了SetPoint公司,并在去年宣布和谷歌合作建立一个名为Galvani Bioelectronics的合资企业,进行一系列疗法的研发,包括炎症性疾病的治疗方法。
迷走神经刺激疗法能否不负众望还有待验证。迄今为止,接受过治疗的人数还非常少,已经完成的两项临床试验中总共只有25名被试。在早期临床试验中看起来前景无限的疗法也常常会在大规模试验中惨败。
但自体免疫疾病患者已经开始注意到这种新疗法了。类风湿性关节炎和克罗恩病的治疗手段都有一定风险,也未必对每个人都有效。Katrin是咨询迷走神经刺激术临床试验的一千多人之一。“我无路可走了,”她说,“我想尝试这种疗法。”