被寄予厚望的基因疗法可能无法像人们预想的那样彻底解决问题。顶级医学期刊发布的两项临床试验表明,旨在恢复视力的基因疗法会在几年内失效。
这并不算是特别惊人的消息,俄勒冈健康与科学大学的眼病研究者Mark Pennesi说,“这些疾病比较复杂,而这只是第一代基因疗法。”Pennesi正在进行类似的临床试验。
Leber先天黑蒙LCA是一种罕见的遗传性失明,患者在四十岁左右会完全丧失视力。大约10%的LCA是RPE65基因突变引发的,这个基因编码的酶能帮助视网膜细胞生产视紫质(rhodopsin)。视网膜的感光细胞需要这种色素,如果RPE65发生突变,感光细胞就会逐渐死亡。
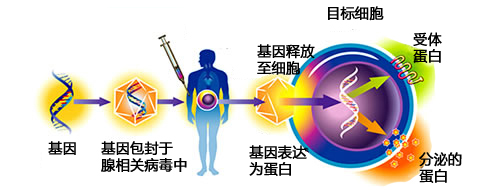
2007年人们首次用基因疗法来治疗失明的盲人,美国和英国有三个独立团队对RPE65型LCA进行了临床试验。医生们将药物注射到患者的眼睛,用无害病毒将一个正常拷贝的RPE65送入视网膜细胞。
许多患者的视网膜在治疗几天后就对光线更为敏感。欣喜若狂的患者将他们的经历公之于众,加拿大患者Dale Turner说他看到的颜色更加鲜明,而纽约男孩Corey Haas经过治疗可以独自骑车、打棒球、阅读字比较大的书。基因疗法也因此受到了广泛的关注。
然而就在两年前,负责美国LCA临床试验的Samuel Jacobson提出了警告。他指出,尽管有15名患者恢复了一定的视力,但他们的感光细胞仍然在恶化。
近日Jacobson等人又在《新英格兰医学》杂志上报告,有三名患者的视力出现下降。研究显示,基因疗法的确提高了视网膜的视觉敏感性,其治疗效果在1到3年内达到顶峰,随后就开始减退。负责英国LCA临床试验的研究团队也在《新英格兰医学》杂志上发表文章指出,虽然12名患者中有6名夜视能力得到提高,但基因疗法的效果在三年内就开始消退。
伦敦大学学院的Robin Ali发现,LCA患者在临床试验中的视力改善远远低于犬类试验。他认为这是因为患者视网膜没有得到足够的RPE65。他的团队正在计划用更强的载体来递送基因,提高RPE65的表达量。但Jacobson等人认为,高剂量可能会带来高毒性,他们倾向于用另一种药物延缓感光细胞的退化。
所幸的是,当年开展的第三个LCA临床试验目前还很顺利。虽然时间已经过了七年半,但基因疗法的效果还很稳定。“现在我们还不能断言治疗效果会不会减弱,不过目前大多数患者视网膜的感光能力得到了持续的改善,”领导这个临床试验的Jean Bennett说。



