CAR-T细胞疗法在经过不断的改良后成了现在治疗癌细胞的疗法。
原标题:CAR-T细胞疗法中CAR设计的新思路
嵌合抗原受体(CAR)是一类工程化的细胞表面受体,一般表达在T细胞上,介导工程化T细胞针对特定靶点肿瘤细胞的杀伤。其中针对CD19(一种B细胞表面标记蛋白)的两款CAR-T细胞疗法Kymriah(诺华)和Yescarta(吉利德)已经于2017年获得了FDA的批准,开创了CAR-T细胞疗法的元年。
近日,纪念斯隆-凯特琳癌症中心的Michel Sadelain及其团队在Nature Medicine上发表的一篇重磅研究指出使用CD3ζ链中的1个ITAM结构域的而不是全长,可以获得更强的肿瘤抑制活性,该研究或将开启未来CAR结构设计的全新思路。
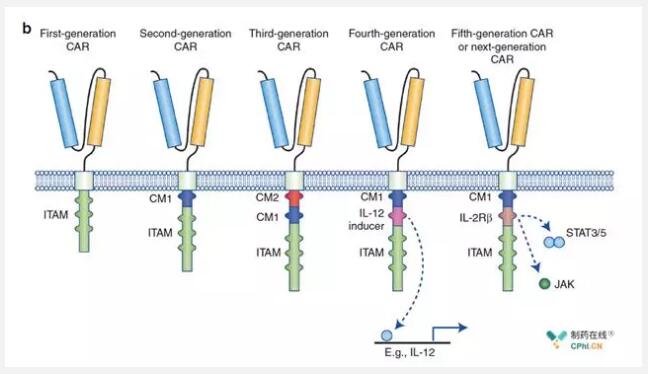
纵观CAR-T的发展史,第一代CAR-T只有CD3ζ链(ITAM,Immunoreceptor Tyrosine-based Activation Motifs);第二代CAR-T添加了CD28或4-1BB等共刺激结构域(CM1),比如Kymriah和Yescarta;第三代CAR-T同时添加了CD28和4-1BB等两个共刺激结构域(CM1和CM2);第四代CAR-T在第二代的基础上添加了共表达的细胞因子,比如IL-12等;第五代CAR-T同样基于第二代,添加了激活其它信号通路的共刺激结构域,比如IL2-2Rβ胞内结合SAAT3/5的结构域。这一代又一代各种不同的结构设计,赋予了CAR-T细胞疗法无限的生机和未来(图1)。
图1:CAR-T细胞结构设计发展历程
上述5代不同设计的CAR-T,虽然都是工程化组合不同信号分子结构域的结构,但仍局限在直接利用原始结构域的范畴内。比如使用CD3ζ链信号传导基序的天然序列(包含3个ITAM),或者使用CD28、4-1BB的胞内信号传导结构域的原始序列,对结构域本身并未做任何工程化改造。特别是CAR设计中最重要的CD3ζ结构域,几乎全都是包含3个ITAM结构域的胞内全长序列。
然而,纪念斯隆-凯特琳癌症中心的Michel Sadelain及其团队在Nature Medicine上发表的一篇重磅研究指出使用CD3ζ链中的1个ITAM结构域的而不是全长,可以获得更强的肿瘤抑制活性,该研究或将开启未来CAR结构设计的全新思路。
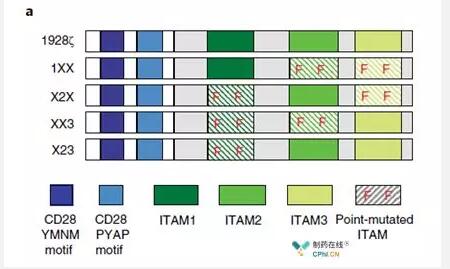
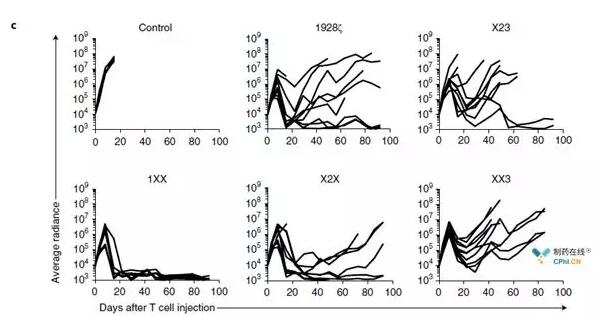
Michel Sadelain及其团队针对使用CD28-CD3ζ的CAR-T细胞较容易出现T细胞耗竭的现象,提出假设认为这可能是由于CD3ζ包含的3个ITAM结构域过度激活T细胞导致的。因此他们基于CD19-CD28-CD3ζ的经典CAR-T结构,设计了3种突变型CD3ζ结构域,分别突变失活了1个或2个ITAM结构域(图2)。结果在小鼠肿瘤模型中发现只有ITAM-1结构域有活性的CAR-T细胞(1XX)体内抗肿瘤活性反而更强,并且具有更长的持久力;而保留ITAM-3结构域活性的CAR-T细胞(XX3)抗肿瘤活性最差(图3)。
图2:不同CD3ζ突变的CD19-CD28-CD3ζ结构,通过点突变技术废除了ITAM结构域的活性
图3:小鼠肿瘤模型评价CAR-T细胞抑制肿瘤细胞的能力
基于上述实验结果,研究者怀疑是不是由于ITAM-3结构域本身传导信号的能力较弱才导致只保留ITAM-3结构域活性的CAR-T细胞效果最差呢?因此他们设计了只含有ITAM-1或ITAM-3的CAR,结果发现它们都可以产生相当的、比经典的CAR-T更强的抑制肿瘤的活性(图4)。这些结果说明在CD19-CD28-CD3ζ结构中,ITAM的数量和所处的位置对CAR-T细胞抑制肿瘤的能力具有重要的影响,越靠近跨膜区的ITAM传导信号的能力越强。
图4:截断CD3ζ的CAR结构设计和小鼠体内肿瘤抑制能力的评价
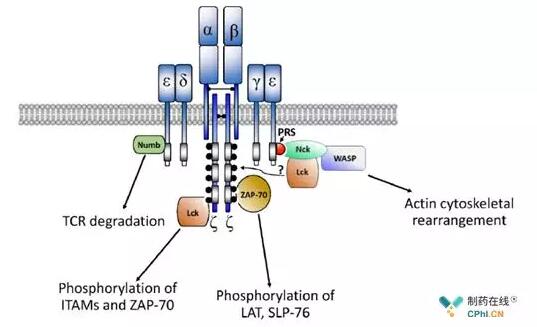
在TCR信号传导中,CD3ζ的激活基序ITAM发挥着关键的作用。简单来说,当TCR-CD3与MHC-peptide结合后,一个叫做Lck的酪氨酸激酶磷酸化CD3ζ的ITAM结构域,磷酸化的ITAM招募并结合ZAP-70蛋白,招募的ZAP-70同样被Lck磷酸化并和Lck一起磷酸化其它的蛋白从而传导T细胞激活信号(图5)。
图5:TCR-CD3信号通路主要相关蛋白
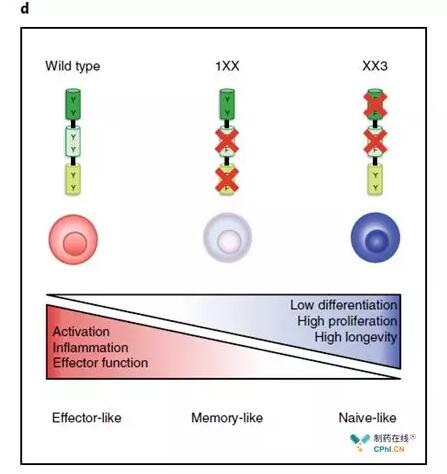
在T细胞的天然激活过程中,CD3ζ的3个ITAM都是不可或缺的,但是为什么在CD19-CD28-CD3ζ结构的CAR-T细胞中只有一个ITAM反而会产生更强的肿瘤抑制活性呢? Michel Sadelain等通过全基因组规模的转录图谱分析发现经典结构的CAR-T细胞更接近效应T细胞,1XX结构的CAR-T细胞更接近于记忆T细胞,而肿瘤抑制活性最差的XX3结构CAR-T细胞更接近于初始T细胞(图6)。所以在体内,同时具备一定效应T细胞和记忆T细胞能力的1XX结构CAR-T细胞具有更持久的肿瘤抑制活性也就不奇怪了。
图6:3种CAR-T细胞表型分析
最后笔者认为,在CD28作为共刺激结构域的CAR设计中,减少ITAM明显具有更强的优势;然而在基于4-1BB作为共刺激结构域的设计中,减少还是增加ITAM更有效果还需要实验验证。但最终的目标都是找到一个最合适的T细胞激活程度,过多或过少都不能发挥最强的肿瘤抑制活性,基于该设计的临床实验也在进行中,我们期待将来会有不错的数据公布。
参考文献:
1. Calibration of CAR activation potential directs alternative T cell fates and therapeutic potency.
2. Selected signalling proteins recruited to the T cell receptor-CD3 complex.
3. Teaching an old dog new tricks: next-generation CAR T cells.
来源:CPhI制药在线
作者:Harry