再生医学网最新获悉,为解决世界器官移植供体严重短缺的问题,相关研究机构决定利用世界先进的
基因编辑技术对猪的基因进行编辑,以生产出可用于人体移植到细胞、组织和器官。
图片来源于网络
器官短缺的危机
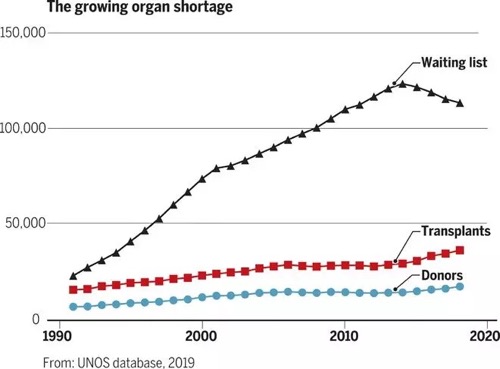
在美国,有超过11万人在等待器官移植来挽救他们的生命,每10分钟就会添加一名新的患者。每天,大约有20名患者因为等不到合适的移植器官而去世。近日在Science Immunology上发表的一篇综述表明,自1990年以来,美国器官移植需求的增长速度远远超过了移植供体和可移植器官的增长速度。在中国,每年有30万适合器官移植方式治疗的患者,但是仅有1万多人能够得到器官移植的救治。
器官短缺的发展趋势
随着器官移植技术的不断完善,它已经成为治疗肾功能衰竭和其它器官疾病患者的重要选择。然而,正是由于器官移植手术的成功率上升,导致了更多患者适于接受这一手术治疗,加剧了移植器官的需求和供给方面的严重失衡。
传统的移植器官来自去世的人群,然而由于大多数去世的人体内的器官并不适合进行移植(据统计只有不到1%的死者的器官可以用于移植),这一途径无法迅速得到扩展,产生足够的器官满足移植手术的需求。
而使用生物工程手段以干细胞或祖细胞为原材料构建或三维打印器官虽然在概念验证上取得了很大的成功,然而目前制造的器官都非常小,还无法在大型动物模型中使用。因此,使用其它哺乳动物(例如猪)的器官进行异种移植可能是解决器官短缺危机的重要近期手段。
异种器官移植面临的挑战和解决办法
在上世纪90年代以来,大多数科学家们的共识是猪是最适合提供异种器官的动物。因为猪的器官与人类器官大小相似,而且具有非常接近的组织学和生理学特征。阻碍猪的器官成功移植到人体的障碍主要是两方面,一方面是人体对异种器官的免疫排斥作用,这包括人体中存在抗体和T/B淋巴细胞对猪器官的排斥。另一个原因是猪携带的一种对猪有益却会传染人类的病毒——猪内源性逆转录病毒(PERV)。这种病毒有可能引发类似HIV的病毒感染。
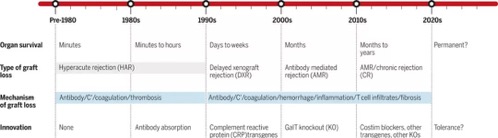
在解决免疫排斥作用方面,过去30年的研究已经取得了长足的进步。通过使用基因工程,科学家们能够在猪的器官中表达调节人体免疫反应的蛋白,敲除猪器官中引起人体免疫排斥反应的抗原。在非人灵长类模型中,猪的移植器官的存活时间从最初的几分钟,延长到了几天、几个月。
提高异种器官存活时间方面的进展
去年《自然》杂志上发布的一项研究中,德国慕尼黑大学(LMU Munich)的一支研究团队将通过基因工程改造的猪心脏移植到狒狒的体内。他们敲除了编码半乳糖基转移酶(galactosyltransferase)的基因,防止猪心脏产生导致急性免疫排斥反应的多糖,然后添加了表达人类CD46蛋白和血栓调节蛋白(thrombomodulin)的基因。CD46能够帮助抑制免疫系统的过激反应,而血栓调节蛋白可以防止导致移植器官死亡的血栓的产生。
实验结果表明,猪的心脏在狒狒体内最长存活到了195天,打破了猪心脏在狒狒体内存活时间的纪录。研究人员表示,使用更好的免疫抑制手段,他们有望将猪心脏的存活时间提高到1年。这将为在开展人体试验铺平道路。
CRISPR基因编辑技术助力攻克PERV感染难题
eGenesis公司和启函生物则利用CRISPR基因编辑技术,在解决PERV感染问题上获得了突破。在2017年,eGenesis的研发团队发表在《科学》杂志上的论文表明,使用CRISPR-Cas9技术,研究人员可以精准地让猪的原代细胞系(porcine primary cell line)中的所有PERV序列失活,随后培育出的小猪体内的PERV序列继续处于失活状态。这意味着,猪携带的PERV病毒序列可能带来的安全隐患,得到了成功的解决。这一研究产生的小猪“莱卡”也登上了《科学》杂志的封面。
《科学》杂志封面
CRISPR基因编辑的另一个优势在于,它可以高通量对猪的基因组进行编辑,除了让PERV序列失活以外,还可以用于解决上面提到的免疫排斥问题。eGenesis和启函生物的研究团队目前已经能够使用CRISPR基因编辑技术,在猪的基因组中更改几十处基因序列。这一技术有望更为快速、安全地完成对猪基因组的修改,产生适用于移植到人体的器官。
除了免疫排斥和PERV病毒感染问题以外,将猪器官移植到人体还需要解决的是器官大小的问题。在狒狒中的试验表明,移植到狒狒中的猪心脏会继续生长,比通常狒狒的心脏要重62%。这会挤压其它维持生命的器官,并且导致动物的死亡。不过科学家们在这方面也取得了进展,前面提到的德国团队使用CRISPR基因编辑技术,将猪生长激素受体(GHR)基因关闭。这种方法能够将猪的重量从原先的360斤降到150斤左右,与人类的体重更为接近。
没有器官短缺的世界
目前,多个研究团队已经接近开展临床试验,检验猪器官在人体中的表现。eGenesis公司进展最快的研究项目是开发用于肾脏移植的猪肾脏。而德国慕尼黑大学的研究团队已经拥有成产无菌猪器官的开发中心,他们开展的第一项临床试验可能是将猪心脏用于延长具有先天性心脏畸形儿童的生命。目前,这些新生儿可能需要等待超过3个月的时间才能获得一颗新的心脏,而在这三个月里,他们的死亡率超过50%。即使移植到体内的猪心脏无法伴随患者一生,它们也可以为这些儿童争取到宝贵的时间。
eGenesis的联合创始人兼首席科学官杨璐菡博士曾经说:“我们正在努力创造一个告别器官短缺的世界。我们终于拥有了解决以前无法解决的问题的工具。”虽然还有很多问题需要解决,但是“无论如何,我们有责任将前沿科学转化为医学,挽救所有等待救治的患者。“
让我们共同期待这项研究能够早日实现,早日告别器官移植短缺的问题,为有需求的患者提供最佳的供体。