当一块肌肉生长时,这块肌肉中的一些干细胞会发育成新的肌肉细胞。这是因为它的主人正在成长或定期锻炼。当受伤的肌肉开始愈合时,也会发生同样的事情。然而与此同时,肌肉干细胞必须产生更多的干细胞,也就是自我更新,否则它们的供给会很快耗尽。这就需要各种参与肌肉生长的细胞相互交流。
再生医学网了解到,两年前,来自德国柏林Helmholtz联合会Max Delbrück分子医学中心(MDC)的Carmen Birchmeier教授领导的研究小组表明,干细胞发育成肌细胞的过程受两种蛋白质的调控,这两种蛋白质是Hes1和MyoD,它们是在祖细胞中以一种振荡的方式产生的,换言之,这些细胞产生的数量存在周期性的波动。
这两种蛋白都参与了Notch信号通路,这是一种广泛的细胞响应外界刺激并与其他细胞通信的机制。该信号通路以其受体“Notch”命名,配体“Delta”(一种细胞表面蛋白)附着在其上。
在近期一项研究中,Birchmeier和MDC的其他四位科学家与来自日本和法国的研究人员一起发现了第三种蛋白质的关键作用,它与Hes1和MyoD一起,在细胞内形成了一个动态网络。相关研究发表在Nature Communications杂志上,标题为Oscillations of Delta-like1 regulate the balance between differentiation and maintenance of muscle stem cells。
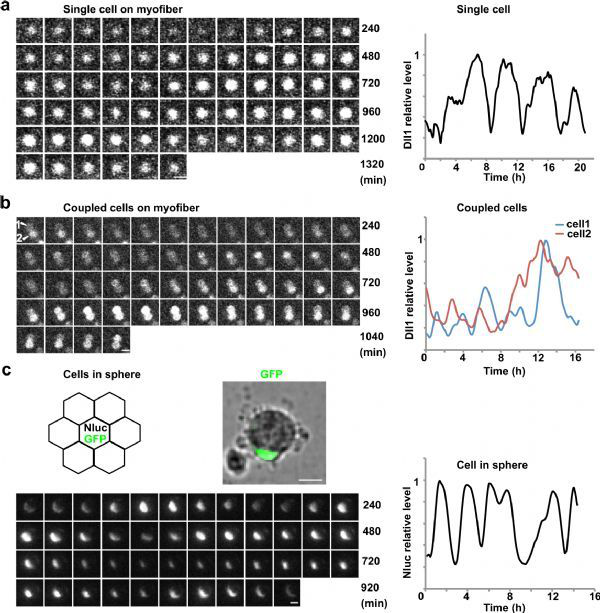
这篇报告中称,这种蛋白质是Notch配体Delta-like1,简称Dll1。“激活的肌肉干细胞以周期性波动的方式产生Dll1,振荡周期持续两到三个小时。每当一部分干细胞表达更多Dll1时,其他细胞中的数量就相应减少。”这种节律性信号决定了干细胞是成为新的干细胞还是发育成肌肉细胞。”Birchmeier解释道。
“只有当Dll1以振荡的方式与Notch受体结合,从而周期性地在干细胞中启动信号级联时,细胞中的自我更新和分化之间才有一个良好的平衡,”Birchmeier总结道。MDC的研究人员希望,对肌肉再生和生长的更好理解,将在有一天能帮助创造出更有效的治疗肌肉损伤和疾病的方法。
(备注:部分图片源自网络。)




