DESTINY-Lung02 II期试验的主要分析结果显示,
德曲妥珠单抗(trastuzumab deruxtecan)在经治的存在HER2突变不可切除和/或转移性非鳞非小细胞肺癌患者中继续展现出强烈且持久的肿瘤缓解。
这些结果以及关于无进展生存期(PFS)和总生存期(OS)的首次报告于今日在国际肺癌研究协会(IASLC)举办的2023年世界肺癌大会(WCLC)上发布(摘要#MA13.10)并同时发表在《临床肿瘤学杂志》上。
德曲妥珠单抗是由
阿斯利康和第一三共联合开发的一种独特设计靶向HER2的抗体偶联药物(ADC)。
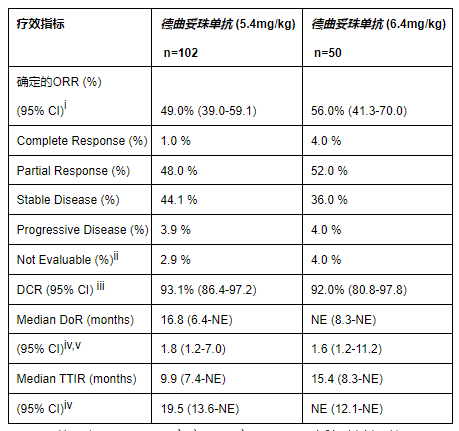
在主要分析中,经盲法独立中央审查(BICR)评估,5.4mg/kg组和6.4mg/kg组的客观缓解率(ORR)分别为49.0%和56.0%。两种剂量的安全性与德曲妥珠单抗的总体安全性一致,5.4mg/kg剂量在该患者群体中显示出良好的安全性。
次要终点的数据也鼓舞人心,根据BICR评估,5.4mg/kg组和6.4mg/kg组的中位PFS分别为9.9个月和15.4个月。在本次分析中,5.4mg/kg组的中位OS为19.5个月,而6.4mg/kg组尚未达到。
美国Dana-Farber癌症研究所Lowe胸部肿瘤中心和Belfer癌症应用科学中心主任Pasi A.J?nne博士表示:"DESTINY-Lung02的主要结果表明,德曲妥珠单抗对接受任一剂量治疗的患者均持续表现出强烈且持久的肿瘤缓解。5.4mg/kg剂量的良好安全性将继续支持德曲妥珠单抗用于治疗HER2突变的非小细胞肺癌,这是一种侵袭性特别强的疾病,患者预后差,过去几乎没什么治疗选择。"
阿斯利康全球执行副总裁、肿瘤治疗领域研发负责人Susan Galbraith表示:"DESTINY-Lung02的研究结果凸显了HER2是肺癌的驱动靶点之一,并强化了在诊断时检测预测性
生物标志物,包括HER2突变的重要性,从而准确识别那些可能获益于靶向治疗的患者。这些数据也再一次展现了我们对德曲妥珠单抗的信心。对于过去几乎没什么选择的患者而言,德曲妥珠单抗是一种潜在的新的靶向治疗选择。"
第一三共全球研发负责人Ken Takeshita表示:"DESTINY-Lung02试验的主要分析中,超过90%的经治HER2阳性非小细胞肺癌患者实现了疾病控制,这强化了我们曾看到德曲妥珠单抗在这种难治疾病中的疗效。这一结果,伴随鼓舞人心无进展生存期和总生存期的首次发布,证实了德曲妥珠单抗可作为该患者群体一个潜在的重要治疗选择"。
DESTINY-Lung02初步分析摘要
CI,置信区间;DCR,疾病控制率;DoR,缓解持续时间;NE,不可估;ORR,客观缓解率;OS,总生存;PFS,无进展生存;TTIR,中位初始应答时间
数据截止:到2022年12月23日
i根据RECIST v1.1,由BICR评估有确定CR或PR的患者比例
ii三名患者在5.4mg/kg剂量下为NE(一名患者因COVID-19从未接受过治疗;两名患者在第一次肿瘤评估前停药);两名患者在6.4mg/kg剂量下为NE(由于首次肿瘤评估前的不良事件而停药)。
iii由BICR评估有确定的CR、PR或SD的患者比例
iv由BICR评估
v 5.4 mg/kg组和6.4 mg/kg组中60.0%和75.0%的患者被设限
vi 5.4 mg/kg组和6.4 mg/kg组中56.9%和60.0%的患者被设限
vii 5.4 mg/kg组和6.4 mg/kg组中63.7%和72.0%的患者被设限
在DESTINY-Lung02中,任一剂量的德曲妥珠单抗均未观察到新的安全性信号。德曲妥珠单抗5.4mg/kg组与6.4mg/kg组相比,3级或更高级别的治疗期间出现的不良事件(TEAE)较低,发生率分别占所有患者中的38.6%和58.0%。最常见的3级或以上的TEAE是中性粒细胞减少症(18.8%(5.4mg/kg);36.0%(6.4mg/kg))和贫血(10.9%(5.4mg/kg);16.0%(6.4mg/kg))。
根据独立评审委员会的决定,有27例病例(5.4mg/kg组中有12.9%,6.4mg/kg组中有28%)报告了与治疗相关的间质性肺病(ILD)或肺炎。在5.4mg/kg组中,大多数ILD病例为低级别(1级或2级)(10.9%),观察到一例3级事件(1.0%),没有观察到4级事件,有一例5级事件(1.0%)。在6.4mg/kg组中,大多数ILD病例也为低级别(26.0%),没有报告3级或4级事件,仅报告了一例5级事件(2.0%)。
关于HER2m的非小细胞肺癌
肺癌是全球第二大常见癌症,2020年诊断出的患者数量超过200万1。转移性非小细胞肺癌患者的预后尤其差,因为只有约9%的患者在诊断后能活过五年以上2。
HER2是一种酪氨酸激酶受体生长促进蛋白,在多种肿瘤表面表达,包括肺癌、乳腺癌、胃癌和结直肠癌。某些HER2(ERBB2)基因改变(称为HER2突变)已在非鳞非小细胞肺癌患者中被确定为独特的分子靶点,在此类肺癌中约占2%-4%会发生3,4。虽然HER2基因突变可以发生在一系列患者中,但更常见于年轻、女性和从未吸烟的NSCLC患者5。HER2基因突变与癌细胞生长和不良预后独立相关,且脑转移的发生率增加6。新一代测序已经用于识别HER2(ERBB2)突变7,8。
尽管抗HER2治疗在乳腺癌和胃癌中的地位已经确立,但在以色列卫生部(MOH)制药司、日本厚生劳动省以及美国食品药品监督管理局(FDA)加速批准德曲妥珠单抗用于治疗不可切除或转移性HER2突变非小细胞肺癌之前,并没有获批用于非小细胞肺癌的HER2靶向疗法9。
关于DESTINY-Lung02
DESTINY-Lung02是一项全球随机II期试验,旨在评估德曲妥珠单抗治疗HER2m不可切除和/或转移性非小细胞肺癌患者的安全性和疗效,这些患者在接受至少一种抗癌治疗方案(必须包含铂类化疗)期间或之后发生疾病复发或进展。患者按2:1随机接受德曲妥珠单抗5.4mg/kg(n=102)或6.4mg/kg(n=50)。
该试验的主要研究终点是经BICR评估的确定的ORR。次要终点包括由研究者以及BICR评估的确认的疾病控制率DCR、DoR、PFS、OS和安全性。
DESTINY-Lung02试验在亚洲、欧洲和北美在内的多地招募了152名患者。有关试验的更多信息,请访问ClinicalTrials.gov。
关于德曲妥珠单抗
德曲妥珠单抗是一种靶向HER2的ADC。德曲妥珠单抗采用第一三共专有的DXd ADC技术设计,是第一三共肿瘤产品组合中领先的ADC,也是阿斯利康ADC科学平台中最先进的项目。德曲妥珠单抗由人源化抗HER2单克隆抗体通过稳定的可裂解四肽连接子与拓扑异构酶-I抑制剂(喜树碱类衍生物DXd)连接组成。
基于DESTINY-Breast03试验的结果,德曲妥珠单抗(5.4mg/kg)在50多个国家被批准用于既往在转移阶段接受过(或一种或多种)抗HER2治疗方案,或在新辅助治疗期间或辅助治疗之后6个月内出现疾病复发的不可切除或转移性HER2阳性成人乳腺癌患者。
基于DESTINY-Breast04试验的结果,德曲妥珠单抗(5.4mg/kg)在40多个国家被批准用于治疗不可切除或转移性HER2-low(IHC 1+或IHC 2+/ISH阴性)乳腺癌的成人患者,这些患者在转移阶段中接受过一次全身治疗或在完成辅助化疗期间或六个月内疾病复发。
德曲妥珠单抗(5.4mg/kg)已在以色列、日本获批,并在美国加速获批,用于治疗不可切除或转移性非小细胞肺癌成人患者,患者需经过FDA批准的检测确认携带活化HER2(ERBB2)突变,且既往接受过全身治疗。对该适应症的持续批准可能取决于验证性试验中对临床益处的验证和描述。
基于DESTINY-Gastric01和/或DESTINY-Gastric02试验的结果,德曲妥珠单抗(6.4mg/kg)在30多个国家被批准用于治疗接受过以曲妥珠单抗为基础治疗后进展的HER2阳性局部晚期或转移性胃癌或胃食管交界处腺癌成人患者。
关于德曲妥珠单抗临床研发计划
评估T-DXd单药在多种HER2靶向癌症中的疗效和安全性的全面研发计划正在全球范围内进行。联合免疫治疗等其他抗肿瘤治疗的试验也在进行中。
关于与第一三共的合作
阿斯利康和第一三共株式会社(TSE:4568)[简称第一三共]分别于2019年3月就德曲妥珠单抗(靶向HER2的ADC药物)、2020年7月就datopotamab deruxtecan(靶向TROP2的ADC药物)的共同开发和商业化达成全球合作。日本除外,第一三共在日本保有ADC的独家权利。第一三共负责德曲妥珠单抗和datopotamab deruxtecan的制造和供应。
关于阿斯利康在肺癌领域的研究
阿斯利康正致力于通过早诊早治提高肺癌患者的治愈率,同时推动相关技术不断向前发展,以改善耐药患者和晚期患者的治疗结局。通过定义新的治疗靶点和评价创新疗法,阿斯利康致力于实现将最合适的药物用于能最大化获益的患者。
公司丰富的产品组合包括领先的肺癌药物以及下一阶段的创新药物,包括奥希替尼和吉非替尼;度伐利尤单抗和tremelimumab;与第一三共合作开发研发的德曲妥珠单抗和datopotamab deruxtecan;与和黄医药合作开发的赛沃替尼;以及横跨各种作用机制的新药及其组合的产品管线。
阿斯利康是全球Lung Ambition Alliance的创始成员,该全球性联盟致力于加快创新步伐,并为肺癌患者提供包括治疗和治疗以外的具有意义的改善措施。
关于阿斯利康在肿瘤领域的研究
阿斯利康正引领着肿瘤领域的一场革命,致力提供多元化的肿瘤治疗方案,以科学探索肿瘤领域的复杂性,发现、研发并向患者提供改变生命的药物。
阿斯利康的肿瘤业务专注于最具挑战性的肿瘤疾病,通过持续不断的创新,阿斯利康已经建立了领先全行业的多元化产品组合和渠道,持续推动医疗实践变革,改变患者体验。
阿斯利康的愿景旨在重新定义癌症治疗,以期未来终结癌症这一致死之因。
关于阿斯利康
阿斯利康(LSE/STO/纳斯达克:AZN)是一家以科学为主导的全球性生物制药公司,专注于肿瘤学、罕见病和生物制药领域处方药的发现、开发和商业化包括心血管、肾脏与代谢、呼吸与免疫学。阿斯利康总部位于英国剑桥,在100多个国家开展业务,其创新药物为全球数百万患者所使用。请访问astrazeneca.com并在社交媒体上关注 AstraZeneca。
声明:本文可能涉及尚未在中国获批的产品或适应症,阿斯利康不推荐任何未被批准的药品使用。
References
参考文献
1.WHO.International Agency of Cancer Research.Cancer Today.2020.Available at:https://gco.iarc.fr/today/home.Accessed September 2023.
2.American Cancer Society.Lung Cancer Survival Rates.Available at:https://www.cancer.org/cancer/lung-cancer/detection-diagnosis-staging/survival-rates.html.Accessed September 2023.
3.Liu S,et al.Targeting HER2 Aberrations in Non–Small Cell Lung Cancer with Osimertinib.Clin Cancer Res.2018;24(11);2594-2604.
4.Riudavets M,et al.Targeting HER2 in non-small-cell lung cancer(NSCLC):a glimpse of hope?An updated review on therapeutic strategies in NSCLC harbouring HER2 alterations.ESMO Open.2021;6(5):100260.
5.Pillai RN,et al.HER2 mutations in lung adenocarcinomas:A report from the Lung Cancer Mutation Consortium.Cancer.2017;123:4099-105.
6.Offin M,et al.Frequency and Outcomes of Brain Metastases in Patients With HER2-Mutant Lung Cancers.Cancer.2019;125:4380-7.
7.Hechtman,J,et al.The Past,Present,and Future of HER2(ERBB2)in Cancer:Approaches to Molecular Testing and an Evolving Role in Targeted Therapy.Cancer Cyto.2019;127(7):428-431.
8.Gulilat M,et al.Targeted next generation sequencing as a tool for precision medicine.BMC Medical Genomics.2019;12(81).
9.Zhou J,et al.Clinical outcomes of patients with HER2-mutant advanced lung cancer:chemotherapies versus HER2-directed therapies.Ther Adv Med Oncol.2020;12.